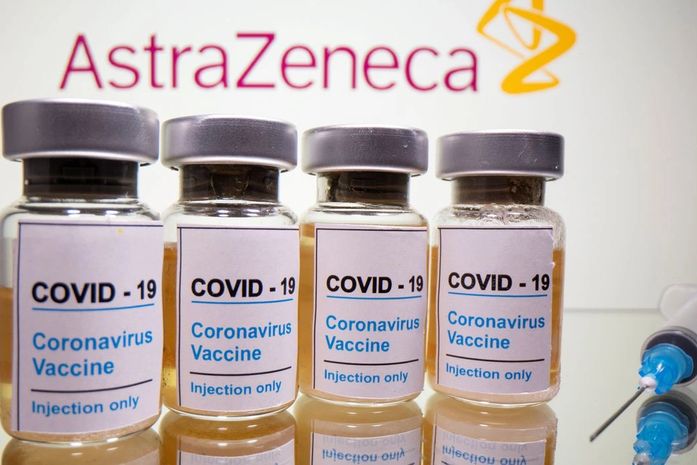
A Fundação Oswaldo Cruz (Fiocruz) solicitou nesta sexta-feira (8) à Agência Nacional de Vigilância Sanitária (Anvisa) o registro de uso emergencial da vacina contra a Covid-19 desenvolvida pela farmacêutica AstraZeneca em parceria com a Universidade de Oxford.
O objetivo da fundação é conseguir autorização para o uso de 2 milhões de doses prontas do imunizante que serão importados da Índia nos próximos dias.
No Brasil, a Fiocruz deve produzir no primeiro semestre deste ano até 100 milhões de doses do imunizante a partir do Ingrediente Farmacêutico Ativo (IFA), que também será importado. No segundo semestre, outras 110 milhões de doses devem ser produzidas inteiramente no Instituto de Tecnologia em Imunobiológicos (Bio-Manguinhos), vinculado à fundação.
A previsão é de que a primeira entrega da produção pela Fiocruz seja de 1 milhão de doses, na semana entre 8 e 12 de fevereiro. Após feito o controle de qualidade e ajustada a produção, a tendência é de que a fabricação aumente, até chegar a 15 milhões de doses por mês.
As vacinas precisam ser armazenadas a uma temperatura entre 2°C e 8°C, o que permite que isso seja feito em geladeiras, simplificando a logística.
Em 31 de dezembro de 2020, a Anvisa aprovou um pedido de importação excepcional de 2 milhões de doses prontas da Índia pela Fiocruz, responsável por produzir a vacina de Oxford no Brasil, poucos dias depois que a substância recebeu da Anvisa a certificação de boas práticas de fabricação.
O Reino Unido foi o primeiro país a aprovar o imunizante da Oxford. Por lá, a prioridade na vacinação é aplicar a primeira de duas doses no maior número de pessoas possível, antes de uma segunda dose até 3 meses depois.
A vacina pode ser 80% eficaz quando há esse intervalo de três meses entre a aplicação das doses, segundo um funcionário envolvido na aprovação no país.